|
| ||||||
| |||||||
| / Обзоры и публикации |
Mucin-17 / MUC17 - мишень для иммунной терапии опухолей желудкаПо последним данным муцины играют решающую роль в образовании опухолей, клеточной адгезии, иммунном ответе и клеточных сигнальных путях. Некоторые муцины, такие как MUC1, MUC16 стали мишенями для иммунотерапии опухолей. Согласно данным ClinicalTrials, новое исследование, основанное на мишени MUC17 (AMG199), в настоящее время находится в фазе I (NCT04117958), при котором оценивают AMG 199 у пациентов с MUC17-положительным раком желудка и гастроэзофагеального соединения (G / GEJ). Это первое клиническое испытание для идентификации MUC17 в качестве потенциальной противоопухолевой мишени.
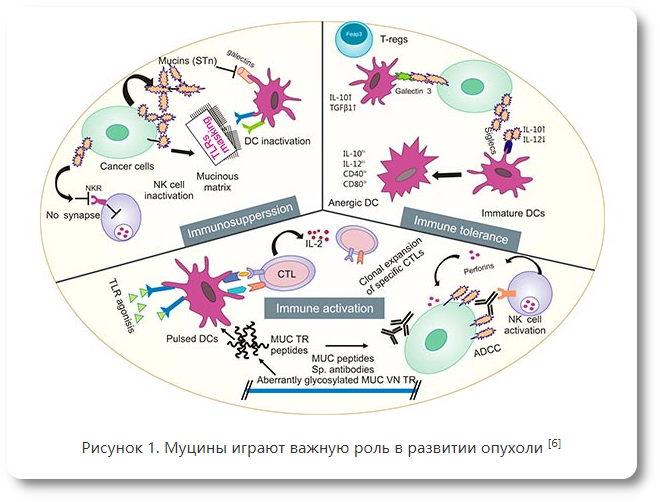
Что такое муцины?Муцины (MUC) представляют собой высокомолекулярные гликопротеины, которые вырабатываются различными эпителиальными клетками. MUC являются основными макромолекулярными компонентами слизи. На сегодняшний день идентифицировано 22 члена Mucin. Муцины классифицируются на мембранно-связанные муцины: MUC1, MUC3A, MUC3B, MUC4, MUC12, MUC13, MUC14, MUC15, MUC17, MUC16, MUC17, MUC17, MUC20, MUC21, MUC22; секретируемые муцины: MUC2, MUC5AC, MUC5B, MUC6, MUC7, MUC8, MUC9, MUC19 [1-3]. Секретируемые муцины образуют вязкий гель, который функционирует как защитный слой над эпителием и может задерживать частицы и микробы. Мембраносвязанные муцины образуют палочкоподобные структуры через O-гликозилированные тандемные повторяющиеся последовательности в их внеклеточных доменах для создания защитного слоя слизи [3]. Было обнаружено, что многие воспалительные цитокины, такие как IL-1β, IL-4, IL-6, TGF-β, IL-9, IL-13, IFN-γ, TNF-α, опосредуют экспрессию муцина в эпителиальных клетках in vitro. [4-5]. Муцины широко присутствуют на поверхностях слизистой оболочки, которые выстилают органы и ткани организма, такие как пищеварительный тракт, дыхательные пути и эпителиальные клетки печени, поджелудочной железы и почек. [3-4]. Некоторые исследования показали, что муцины могут быть использованы в качестве потенциального инструмента для прогнозирования восприимчивости к COVID-19. [5]. Некоторые муцины участвуют в различных сигнальных путях, связанных с трансформацией и прогрессированием опухоли. Поэтому ожидается рост интереса к муцинам в диагностике и прогнозе опухолей, так же в качестве потенциальной мишени для лечения опухолей (рисунок 1).) [6-10].
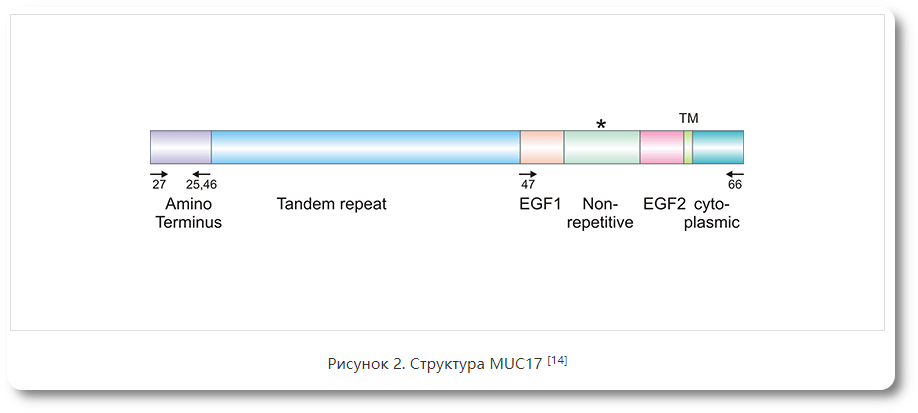
Структура MUC17Муцин-17 (MUC17, также известный как MUC3) является трансмембранным муцином, кодируемым геном MUC17, расположенным в области 7q22. Муцины структурно разнообразны, но имеют сходные структурные особенности. Длинный внеклеточный домен MUC17 может потенциально влиять на клеточную адгезию путем изменения взаимодействия молекул клеточной адгезии и является местом обширного гликозилирования. Цитоплазматический домен имеет много предсказанных участков фосфорилирования, которые могут опосредуть трансдукцию сигнала. Внеклеточный домен определяет MUC-специфическую пространственную структуру и иммуногенность. Роли двух EGF-подобных доменов до конца не изучены (рисунок 2) [11-12, 14].
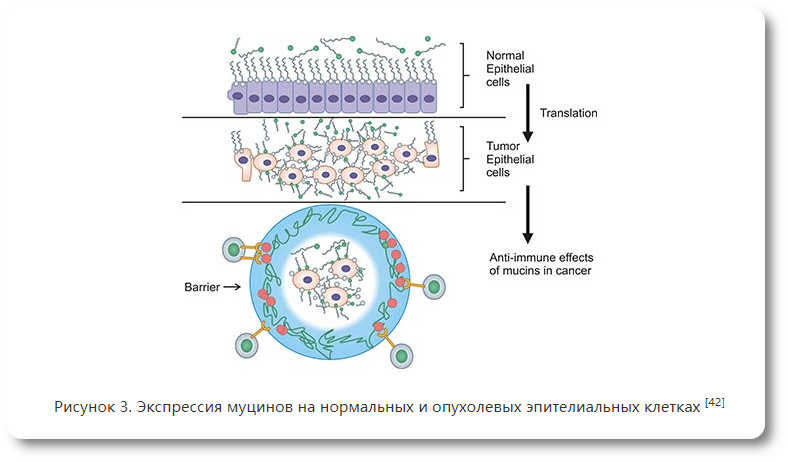
MUC17 в основном экспрессируется в кишечнике и является компонентом кишечной слизи. Экспрессия MUC17 усиливает барьер кишечной слизи и ослабляет воспаление в поврежденных участках слизистой оболочки [11]. Что еще более важно, MUC17 чрезмерно экспрессируется примерно в половине случаев рака желудка. Как правило, муцины экспрессируются на поверхности плотно упакованных столбчатых клеток в нормальном эпителии, которые образуют защитную и смазывающую функцию на слое клеток слизистой оболочки. Однако в злокачественных опухолевых клетках муцины высоко экспрессируются на трансформированных опухолевых клетках и покрывают все поверхностные участки клеточной мембраны, а опухолевые клетки приобретают округлую форму, увеличивают пористость клеток и теряют полярность (рисунок 3).) [42].
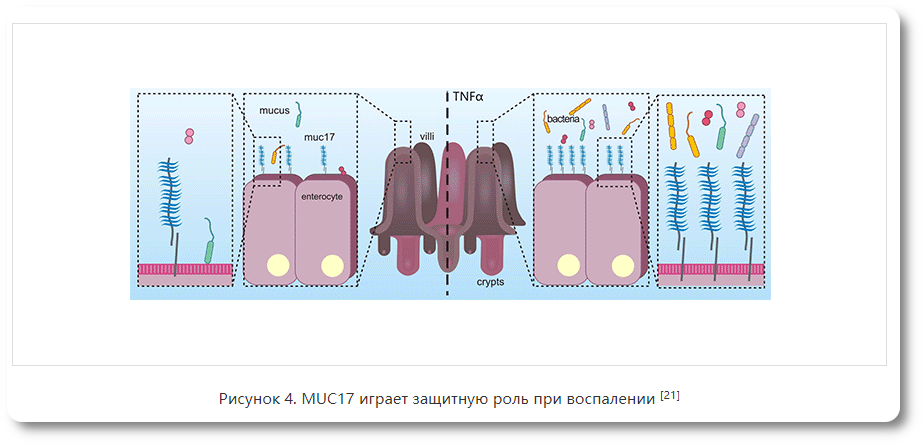
Некоторые результаты показывают, что MUC17 в качестве белка-супрессора рака желудка обладает терапевтическим потенциалом для ГК человека [20, 22]. Кроме того, потеря пунктатного иммуноокрашающего паттерна MUC17 была связана с агрессивным поведением колоректальной аденокарциномы и сокращением выживаемости пациентов. [41]. В отсутствие MUC17 в клетках аденокарциномы поджелудочной железы наблюдалось увеличение массы опухоли. [42]. Эти результаты показали, что MUC17 может подавлять опухоль. Необходимы дальнейшие исследования для определения специфической роли MUC17 в патогенезе этих видов рака. MUC17-опосредованный сигнальный путь трансдукцииКак мембранно-связанный муцин с важными биологическими функциями, уровни экспрессии MUC17 связаны с пролиферацией различных воспалительных и опухолевых клеток, что дает важные подсказки для профилактики и лечения заболеваний, связанных с MUC17, но его молекулярный механизм остается неясным. В клетках аденокарциномы толстой кишки длительная стимуляция провоспалительным цитокином TNFα, который индуцирует воспалительное состояние, может привести к увеличению MUC17, что, в свою очередь, защищает клетки аденокарциномы толстой кишки от адгезии энтеропатогенной E. coli. Результаты показывают, что MUC17 может играть защитную роль при воспалении (рисунок 4).) [21]. Другое исследование показало, что EGF-подобный домен MUC17 активировал путь Rho/Rock через взаимодействующий MYH9, а затем ингибировал путь NFκB, который стимулировался факторами воспаления. MUC17 может ингибировать прогрессирование рака желудка человека, ограничивая воспалительные реакции через регуляторную петлю обратной связи MYH9-p53-RhoA. [22]. Другие отчеты о MUC17 показывают, что C-конец MUC17 связывается с каркасными белками PDZK1, что стабилизирует его локализацию на апикальной мембране энтероцитов тонкой кишки. [23]; Метилирование ДНК и модификации гистона H3K9 способствуют экспрессии MUC17 [24]. Также при раке толстой кишки исследование показало, что MUC17 может связываться с семейством EGFR ERBB2, активируя передачу сигналов Wnt, регулируя процесс EMT. [25-26]. Кроме того, было показано, что синтетический пептид, полученный из молозива, содержащий мотив TFLK, стимулирует повышенную экспрессию MUC17 в клетках клеточной линии толстой кишки HT29. Мотив TFLK представляет собой характерную структурную последовательность белка MSAA3, которая важна для профилактики патогенной бактериальной атаки и защиты желудочно-кишечного тракта у новорожденных. Этот механизм даст новые идеи для усиления кишечного слизевого барьера и предотвращения множественных воспалительных заболеваний. [27-28].
Роль MUC17 в ракеКак трансмембранный муцин, MUC17 играет важную роль в защите от бактериальной атаки. Дерегулированное производство MUC17 было связано с различными типами рака и воспалительными заболеваниями. [29, 30]. В настоящее время большое количество исследований сосредоточено на связи MUC17 с опухолями желудочно-кишечного тракта и другими опухолями, такими как рак толстой кишки, желудка, поджелудочной железы, пищевода и молочной железы. [31-40]. При колоректальном раке, основываясь на иммуногистохимическом анализе, исследователи наблюдали равномерное окрашивание MUC17 в цитоплазме во всех доброкачественных (нормальных) эпителиальных тканях толстой кишки. Тогда как в CRC встречаются только пунктатное окрашивание (60 из 136, 44%), полное отсутствие окрашивания (ноль) или диффузные низкие уровни MUC17 (76 из 136, 56%). Потеря пунктатного иммуноокрашающего паттерна MUC17 была связана с агрессивным поведением CRC и сокращением выживаемости пациентов. Анализы на основе клеток in vitro показали, что клетки со стабильным ингибированием MUC17 siRNA значительно снизили остановку клеточного цикла в фазе G0 / G1 или S. В совокупности серия клеточных экспериментов показала, что MUC17 может быть белковым продуктом потенциального гена-супрессора опухоли при колоректальном раке. [16, 31, 41]. При раке поджелудочной железы MUC17 был чрезмерно экспрессирован в тканях рака поджелудочной железы по сравнению с нормальными тканями поджелудочной железы. Обнаружение тканей аденокарциномы протоков поджелудочной железы с помощью иммуногистохимии выявило значительно улучшенную экспрессию MUC17, предполагая, что MUC17 может быть одним из независимых прогностических факторов [32-33]. Другое исследование показало, что изменения в экспрессии MUC17 положительно коррелируют с развитием пищевода Барретта, аденокарциномы пищевода, кишечной железы и рака поджелудочной железы. [35-37]. При раке молочной железы было обнаружено, что нокдаун MUC17 связан с лекарственной чувствительностью у пациентов, что также показывает, что активность MUC17 и PCNX1 может влиять на устойчивость к химиотерапии, например, делать опухолевые клетки более чувствительными к препаратам. А именно, MUC17 может быть потенциальным биомаркером ответа химиотерапии при раке молочной железы. [25, 38-39]. При раке желудка и гастроэзофагеальном соединении (G/GEJ) было продемонстрировано, что MUC17 чрезмерно экспрессируется на клеточных мембранах G/GEJ. Таким образом, MUC17 рассматривается как опухолеассоциированный антиген (TAA). Рак желудка связан с дисфункцией барьера слизистой оболочки желудка. Повреждение слизистого барьера желудка обычно приводит к хроническому воспалению, которое является основным фактором канцерогенеза желудка. Дальнейшие исследования показали, что когда экспрессия MUC17 снижалась, клоногенная способность уменьшалась. Кроме того, уменьшилось количество опухолеинвазивных клеток, а также миграция клеток и пролиферация клеток. MUC17 Knockdown сдерживал инвазивную и пролиферативную способность клеток рака желудка, предполагая, что MUC17 может быть новой мишенью для терапии рака желудка [40].
Перспективы клинических исследований MUC17Биспецифическое антитело, нацеленное на MUC17 (AMG199; MUC17 x CD3) от Amgen Inc. был исследован в I клиническом испытании, которое предназначено для лечения MUC17-положительных солидных опухолей, включая желудочно-кишечный тракт, гастроэзофагеальный переход, колоректальный рак и рак поджелудочной железы. В 2020 году Amgen Inc. получила fda статус орфанного препарата AMG199. На ежегодном собрании ASCO в 2021 году Компания Amgen объявила о проведении первого открытого исследования фазы I по повышению дозы у людей для оценки дозоограничивающей токсичности и эффективности AMG199 у пациентов с MUC17-положительным G/GEJ и определения максимально переносимой дозы (MTD) и/или рекомендуемой дозы фазы 2 (RP2D). Заявлено, что исследования I фазы будут завершены в марте 2024 года. Многие работы предполагают, что муцины чрезмерно экспрессируются при различных злокачественных опухолях. Роль муцинов в опухолях дает важные подсказки для разработки противоопухолевых препаратов на основе муцина. В связи с этим некоторые муцины функционируют как потенциальные мишени для терапевтических вмешательств при различных видах рака. Между тем, с дальнейшими работами над структурой и функцией MUC17, MUC17 также стал очень привлекательной мишенью для лечения рака. Ожидается, что MUC17 и другие трансмембранные муцины также будут идентифицированы как прямые лекарственные мишени с терапевтической перспективой.
Ссылки [1] Dekker, Jan, et al. "The MUC family: an obituary." Trends in biochemical sciences 27.3 (2002): 126-131. [2] Alcântara, Angélica Leite de, et al. "MUC family influence on acute lymphoblastic leukemia in Native American populations from Brazilian Amazon." (2022): e19025-e19025. [3] Sousa, Andreia M., et al. "Reflections on MUC 1 glycoprotein: the hidden potential of isoforms in carcinogenesis." apmis 124.11 (2016): 913-924. [4] Długosz, Ewa, et al. "Toxocara canis mucins among other excretory-secretory antigens induce in vitro secretion of cytokines by mouse splenocytes." Parasitology research 114.9 (2015): 3365-3371. [5] Lin, Susanne Je-Han, Bailey Arruda, and Eric Burrough. "Alteration of Colonic Mucin Composition and Cytokine Expression in Acute Swine Dysentery." Veterinary Pathology 58.3 (2021): 531-541. [6] Bhatia R, Gautam SK, Cannon A, et al. Cancer-associated mucins: role in immune modulation and metastasis. Cancer Metastasis Rev. 2019;38(1-2):223-236. [7] Brockhausen, Inka, and Jacob Melamed. "Mucins as anti-cancer targets: Perspectives of the glycobiologist." Glycoconjugate Journal 38.4 (2021): 459-474. [8] Marimuthu, Saravanakumar, et al. "Mucins reprogram stemness, metabolism and promote chemoresistance during cancer progression." Cancer and Metastasis Reviews 40.2 (2021): 575-588. [9] Wi, Dong-Han, Jong-Ho Cha, and Youn-Sang Jung. "Mucin in cancer: a stealth cloak for cancer cells." BMB reports 54.7 (2021): 344. [10] Kufe, Donald W. "Mucins in cancer: function, prognosis and therapy." Nature Reviews Cancer 9.12 (2009): 874-885. [11] Shekels LL, Ho SB. Characterization of the mouse Muc3 membrane bound intestinal mucin 5' coding and promoter regions: regulation by inflammatory cytokines. Biochim Biophys Acta. 2003;1627(2-3):90-100. [12] Desseyn, Jean-Luc, Daniel Tetaert, and Valérie Gouyer. "Architecture of the large membrane-bound mucins." Gene 410.2 (2008): 215-222. [13] Gum Jr, James R., et al. "MUC17, a novel membrane-tethered mucin." biochemical and biophysical research communications 291.3 (2002): 466-475. [14] Moniaux, Nicolas, et al. "Characterization of human mucin MUC17: Complete coding sequence and organization." Journal of Biological Chemistry 281.33 (2006): 23676-23685. [15] Schneider, Hannah, et al. "The human transmembrane mucin MUC17 responds to TNFα by increased presentation at the plasma membrane." Biochemical Journal 476.16 (2019): 2281-2295. [16] Senapati, Shantibhusan, et al. "Expression of intestinal MUC17 membrane-bound mucin in inflammatory and neoplastic diseases of the colon." journal of clinical pathology 63.8 (2010): 702-707. [17] Gál, Eleonóra, et al. "Importance of MUC17 in the Bile-Induced Pancreatic Cancer Progression."(2022). [18] Layunta, Elena, et al. "IL-22 promotes the formation of a MUC17 glycocalyx barrier in the postnatal small intestine during weaning." Cell Reports 34.7 (2021): 108757. [19] Bailis, Julie M., et al. "Preclinical evaluation of BiTE® immune therapy targeting MUC17 or CLDN18. 2 for gastric cancer." Cancer Research 80.16_Supplement (2020): 3364-3364. [20] Lordick, F., et al. "P-76 A phase 1 study of AMG 199, a half-life extended bispecific T-cell engager (HLE BiTE®) immune therapy, targeting MUC17 in patients with gastric and gastroesophageal junction cancer." Annals of Oncology 31 (2020): S114. [21] Schneider, Hannah, et al. "The human transmembrane mucin MUC17 responds to TNFα by increased presentation at the plasma membrane." Biochemical Journal 476.16 (2019): 2281-2295. [22] Yang, Bing, et al. "Mucin 17 inhibits the progression of human gastric cancer by limiting inflammatory responses through a MYH9-p53-RhoA regulatory feedback loop." Journal of Experimental & Clinical Cancer Research 38.1 (2019): 1-13. [23] Malmberg, Emily K., et al. "The C-terminus of the transmembrane mucin MUC17 binds to the scaffold protein PDZK1 that stably localizes it to the enterocyte apical membrane in the small intestine." Biochemical Journal 410.2 (2008): 283-289. [24] Kitamoto, Sho, et al. "DNA methylation and histone H3-K9 modifications contribute to MUC17 expression." Glycobiology 21.2 (2011): 247-256. [25] Yu, Kuan, et al. "Intratumoral PD-1+ CD8+ T cells associate poor clinical outcomes and adjuvant chemotherapeutic benefit in gastric cancer." British journal of cancer 127.9 (2022): 1709-1717. [26] Al Amri, Waleed S., et al. "Genomic and Expression Analyses Define MUC17 and PCNX1 as Predictors of Chemotherapy Response in Breast CancerMUC17 and PCNX1 Predict Chemoresponse." molecular cancer therapeutics 19.3 (2020): 945-955. [27] Pan, Qiong, et al. "Enhanced Membrane-tethered Mucin 3 (MUC3) Expression by a Tetrameric Branched Peptide with a Conserved TFLK Motif Inhibits Bacteria Adherence*[S]." Journal of Biological Chemistry 288.8 (2013): 5407-5416. [28] Qiong, P. A. N., et al. "Influence of MSAA3 protein fragment and modified peptide thereof on the MUC3 expression of HT29 cells." Medical Journal of Chinese People's Liberation Army 36.10 (2011): 1062-1064. [29] Resta-Lenert, Silvia, et al. "Muc17 protects intestinal epithelial cells from enteroinvasive E. coli infection by promoting epithelial barrier integrity. "American Journal of Physiology-Gastrointestinal and Liver Physiology 300.6 (2011): G1144-G1155. [30] Yang, Ching-Wen, et al. "Genetic variations of MUC17 are associated with endometriosis development and related infertility." BMC medical genetics 16.1 (2015): 1-7. [31] Jiang, Zhipeng, et al. "Analysis of TGCA data reveals genetic and epigenetic changes and biological function of MUC family genes in colorectal cancer." future Oncology 15.35 (2019): 4031-4043. [32] Kitamoto, Sho, et al. "Expression of MUC17 is regulated by HIF1α-mediated hypoxic responses and requires a methylation-free hypoxia responsible element in pancreatic cancer." (2012): e44108. [33] Kitamoto, Sho, et al. "Expression of MUC17, a marker of pancreatic cancer, is under the control of epigenetic modifications." Cancer Research 71.8_Supplement (2011): 82-82. [34] Hyland, Paula L., et al. "Global changes in gene expression of Barrett's esophagus compared to normal squamous esophagus and gastric cardia tissues." PLoS One 9.4 (2014): e93219. [35] Ye et al. "The role of MUC1, MUC3 and MUC6 in Barrett's esophagus, esophageal adenocarcinoma, cardia intestinal metaplasia and cardia adenocarcinoma." 2006. [36] Glickman, Jonathan N., Aliakbar Shahsafaei, and Robert D. Odze. "Mucin core peptide expression can help differentiate Barrett's esophagus from intestinal metaplasia of the stomach." The American journal of surgical pathology 27.10 (2003): 1357-1365. [37] Lonie, James M., Andrew P. Barbour, and Riccardo Dolcetti. "Understanding the immuno-biology of oesophageal adenocarcinoma: Towards improved therapeutic approaches. "Cancer Treatment Reviews 98 (2021): 102219. [38] Rakha, Emad A., et al. "Expression of mucins (MUC1, MUC2, MUC3, MUC4, MUC5AC and MUC6) and their prognostic significance in human breast cancer." Modern Pathology 18.10 (2005): 1295-1304. [39] Al Amri, W., et al. "Abstract P3-06-19: MUC17 and PCNX1 as mediators of chemotherapy response in breast cancer." Cancer Research 79.4_Supplement (2019): P3-06. [40] Chao, Joseph, et al. "Trial in progress: a phase I study of AMG 199, a half-life extended bispecific T-cell engager (HLE BiTE) immune therapy, targeting MUC17 in patients with gastric and gastroesophageal junction (G/GEJ) cancer." (2020): TPS4649-TPS4649. [41] Katkoori, Venkat, et al. "Abstract# 4362: MUC17 is a potential tumor suppressor gene in colorectal adenocarcinoma." Cancer Research 69.9_Supplement (2009): 4362-4362. [42] Lin, Bo, et al. "Alpha-fetoprotein binding mucin and scavenger receptors: an available bio-target for treating cancer." Frontiers in Oncology 11 (2021): 625936. |
|
|
© ООО «Лабораторная Диагностика» info@LD.ru тел.: +7 495 369-20-43 |